L’ape europea (Apis melliferas) è un insetto impollinatore che ha un ruolo importante nel mantenimento della biodiversità di molteplici specie vegetali. Le api possono essere minacciate non solo dall’intervento dell’uomo, ma anche da agenti biologici, come virus, che possono alterare le colonie. Tra i virus più diffusi nelle api vi rientra il virus delle ali deformi (deformed wing virus – DWV), oggetto di questo articolo.

Caratteristiche del virus delle ali deformi
Il virus delle ali deformi fu isolato per la prima volta nel 1977 in esemplari di api adulte dell’Egitto, da cui assunse inizialmente il nome di virus delle api egizie (EBV). Successivamente, nel 1982 in Giappone, i ricercatori identificarono un virus strettamente correlato all’EBV e, visti i segni clinici, attribuirono il nome di virus delle ali deformi. Il nome tassonomico attribuito al DWV è Iflavirus aladeformis, appartenente all’ordine dei Picornavirales e alla famiglia degli Iflaviridae.
Ad oggi il DWV ha una distribuzione globale e colpisce sia diverse specie di api che i bombi. Inoltre, la sua ampia presenza lo rende tra i patogeni più importanti in grado di infettare le api, soprattutto per i danni che può causare all’insetto.
La diffusione del DWV è associata a Varroa destructor, acaro parassita che necessita delle api per completare il suo ciclo riproduttivo. La presenza stagionale dell’acaro (primavera/estate) aumenta la probabilità di diffusione del virus: l’acaro parassitando l’ape infetta, entra in contatto con il DWV diventando un vettore di diffusione.
Filogenesi
| Dominio | Riboviria |
| Regno | Orthornavirae |
| Phylum | Pisuviricota |
| Classe | Pisoniviricetes |
| Ordine | Picornavirales |
| Famiglia | Iflaviridae |
| Genere | Iflavirus |
| Specie | Iflavirus aladeformis |
Struttura del DWV
Il virus delle ali deformi presenta particelle virali (dette virioni) icosaedriche (20 facce) di circa 30 nm di diametro. All’interno del virione si trova il genoma, costituito da un singolo filamento positivo di RNA (+ssRNA) lungo circa 10.000 nucleotidi. Questo filamento si definisce “positivo” in quanto viene direttamente utilizzato come stampo per creare l’RNA messaggero (mRNA).
Le proteine strutturali principali che compongono il guscio del virione (capside) sono VP0 (formata da VP2 e VP4), VP1 e VP3. Tutte le proteine sintetizzate dal DWV sono prodotte come unica poliproteina, e successivamente sono tagliate per formare le proteine attive.
Le proteine strutturali si assemblano in unità base chiamate protomeri, ovvero i mattoncini strutturali. Sessanta di questi protomeri si uniscono formando un guscio proteico icosaedrico, organizzato in 12 gruppi da 5 protomeri ciascuno. Il capside del DWV esternamente è formato principalmente dalla proteina VP1, a cui seguono VP3 e VP2; mentre VP4 si trova nello strato interno.
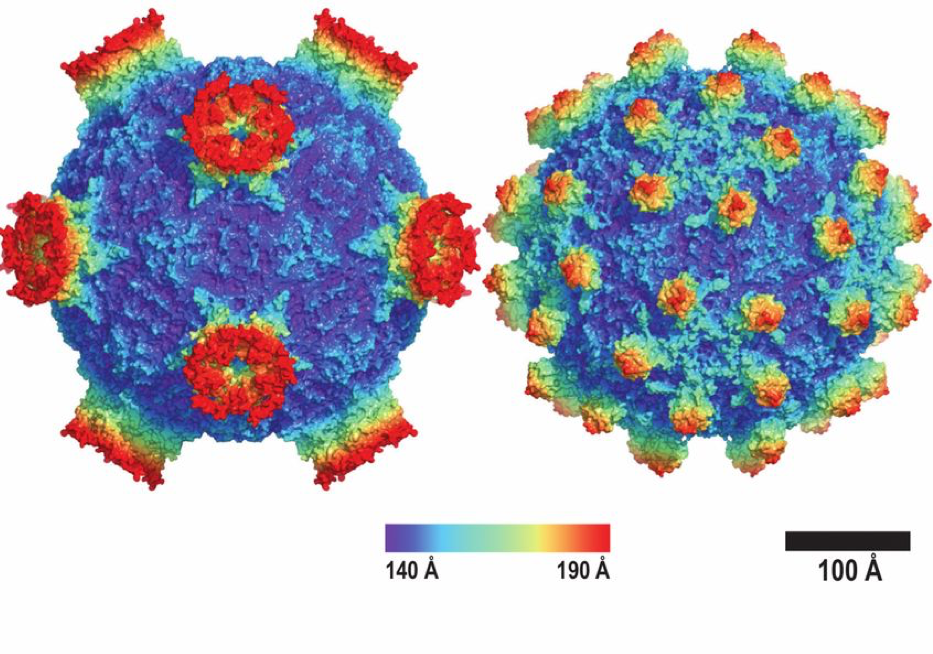
[Fonte: Skubník et al., 2017]
Il meccanismo di ingresso degli Inflavirus, e quindi anche del virus delle ali deformi, non è ben noto. Si pensa che si tratti di endocitosi mediata da recettore, ossia un meccanismo che sfrutta l’invaginazione della membrana cellulare. Pertanto, il ruolo delle proteine strutturali appare fondamentale per consentirne l’ingresso.
Si ipotizza che la proteina VP3, con il suo dominio P, potrebbe svolgere un ruolo nell’interazione del virus con la membrana. Invece, vista la sua posizione interna, la proteina VP4 potrebbe creare dei pori nella membrana cellulare e facilitare lo spostamento del genoma del DWV.
Genoma del DWV
Il genoma del DWV contiene un’unica open reading frame (ORF), ovvero una sequenza continua di nucleotidi che viene tradotta come singola poliproteina. Infatti, questa sequenza porta l’informazione genetica per la codifica delle componenti strutturali e non. Una regione non tradotta fiancheggia l’ORF sia al 5’UTR che al 3’UTR. Inoltre, al 5’UTR è presente un sito interno di ingresso del ribosoma (IRES), che consente di reclutare il ribosoma dell’ospite per iniziare la traduzione.
Le proteine strutturali precedentemente citate, si localizzano nel genoma del DWV in successione alla regione IRES e sono precedute dal polipeptide leader (Lp). Seguono poi le proteine non strutturali: l’elicasi, la proteasi 3C e una RNA-polimerasi RNA-dipendente (RdRp). L’elicasi e la RdRp sono fondamentali per la replicazione del genoma virale, mentre la proteasi consente il taglio della poliproteina nelle varie proteine.
Il virus delle ali deformi, avendo un genoma a RNA, è di conseguenza soggetto a variabilità genetica. Infatti, il complesso replicativo dei virus a RNA è meno preciso e la RdRp può facilmente sbagliare. Si originano così mutazioni cumulabili, con conseguente formazione di varianti virali (come il tipo A, B e C).

Immagini al microscopio
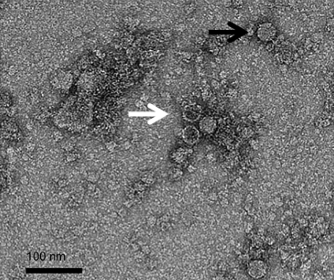
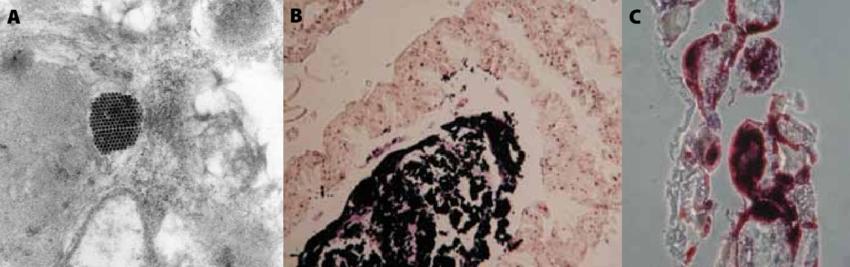
Patogenesi del DWV
Il virus in questione può avere trasmissione verticale o orizzontale. Nel primo caso, la trasmissione avviene tramite le uova e lo sperma del fuco, portando la nascita di larve infette. Nel secondo caso, le api possono venire a contatto con il virus tramite cibo contaminato, scambio di cibo tra loro (trofallassi) o mangiando pupe infette durante il comportamento igienico.
Anche l’acaro V. destructor può essere un mezzo di trasmissione del DWV. Infatti, infestando la colonia e nutrendosi dell’emolinfa delle api può diffondere velocemente il virus su altre colonie sane.
Queste vie sono utilizzate dal virus delle ali deformi per entrare nell’ape e localizzarsi in diversi tessuti, come ovaie, spermateca, tessuto adiposo ed intestino. Da qui porta avanti il meccanismo della replicazione, con ottenimento di molteplici virioni maturi.
In genere, la sintomatologia legata al virus in esame non è visibile, ma appare grave solo in associazione con l’acaro Varroa. In questa condizione, DWV porta a morte delle pupe, deformità delle ali dell’ape e addomi gonfi e accorciati. Inoltre, le api possono apparire sane ma con problematiche a livello del sistema nervoso centrale. Questi sintomi portano conseguentemente al collasso della colonia.

[Fonte: de Miranda et al., 2011]
Metodi di identificazione
Il virus delle ali deformi può essere identificato tramite valutazione della sintomatologia o specificatamente con tecniche immunologiche per identificare anticorpi (test ELISA). Un altro metodo molecolare è la RT-qPCR, che valuta la presenza del genoma virale nell’ospite. Mentre, la presenza del DWV nei tessuti è analizzata tramite ibridazione in situ (ISH).
Terapie
Ad oggi non sono disponibili terapie antivirali per api infette e tantomeno non sono presenti vaccini per proteggerle da DWV. Il controllo del virus si basa principalmente sulla gestione dell’acaro V. destructor, tramite trattamenti mirati, e su strategie preventive. Queste limitazioni rendono quindi il virus delle ali deformi una problematica di notevole importanza per gli apicoltori e per il mantenimento della biodiversità.
Applicazioni biotecnologiche
Recentemente, i ricercatori hanno condotto studi riguardanti il DWV basati sull’uso del meccanismo naturale di silenziamento genico specifico: l’interferenza dell’RNA. Questo sistema è in grado di riconoscere RNA a doppio filamento (come quello della replicazione virale) e di processarlo creando dei siRNA, frammenti più piccoli. Queste ricerche hanno mostrato come l’inoculazione di dsRNA specifico di DWV possa portare a riduzione dell’infezione, suggerendo una nuova strategia terapeutica. Per concludere, questa tecnologia, sfruttando un meccanismo naturale di difesa, rappresenta un approccio innovativo e mirato che potrebbe essere usato per contrastare il virus delle ali deformi.
Fonti
- https://www.ncbi.nlm.nih.gov/datasets/taxonomy/tree/?taxon=3047792
- De Miranda, J. R., Gauthier, L., Ribiere, M., & Chen, Y. P. (2011). Honey bee viruses and their effect on bee and colony health. In Honey Bee Colony Health: Challenges and Sustainable Solutions (pp. 71–102).
- Lanzi, G., de Miranda, J. R., Boniotti, M. B., Cameron, C. E., Lavazza, A., Capucci, L., Camazine, S. M., & Rossi, C. (2006). Molecular and biological characterization of deformed wing virus of honeybees (Apis mellifera L.). Journal of virology, 80(10), 4998–5009.
- Norton, A. M., Remnant, E. J., Buchmann, G., & Beekman, M. (2020). Accumulation and Competition Amongst Deformed Wing Virus Genotypes in Naïve Australian Honeybees Provides Insight Into the Increasing Global Prevalence of Genotype B. Frontiers in microbiology, 11, 620.
- de Miranda JR, Genersch E. Deformed wing virus. J Invertebr Pathol. 2010 Jan;103 Suppl 1:S48-61.
- Organtini LJ, Shingler KL, Ashley RE, Capaldi EA, Durrani K, Dryden KA, Makhov AM, Conway JF, Pizzorno MC, Hafenstein S. Honey Bee Deformed Wing Virus Structures Reveal that Conformational Changes Accompany Genome Release. J Virol. 2017 Jan 3;91(2):e01795-16.
- Škubník K, Nováček J, Füzik T, Přidal A, Paxton RJ, Plevka P. Structure of deformed wing virus, a major honey bee pathogen. Proc Natl Acad Sci U S A. 2017 Mar 21;114(12):3210-3215.
- Gisder S, Genersch E. Viruses of commercialized insect pollinators. J Invertebr Pathol. 2017 Jul;147:51-59.
- Smeele ZE, Baty JW, Lester PJ. Effects of Deformed Wing Virus-Targeting dsRNA on Viral Loads in Bees Parasitised and Non-Parasitised by Varroa destructor. Viruses. 2023 Nov 15;15(11):2259.
Fonti immagini
- Figura 1: https://www.wwf.it/cosa-puoi-fare-tu/ecotips/cose-che-forse-non-sai-sulle-api/
- Figura 2: Škubník K, Nováček J, Füzik T, Přidal A, Paxton RJ, Plevka P. Structure of deformed wing virus, a major honey bee pathogen. Proc Natl Acad Sci U S A. 2017 Mar 21;114(12):3210-3215.
- Figura 3: Norton, A. M., Remnant, E. J., Buchmann, G., & Beekman, M. (2020). Accumulation and Competition Amongst Deformed Wing Virus Genotypes in Naïve Australian Honeybees Provides Insight Into the Increasing Global Prevalence of Genotype B. Frontiers in microbiology, 11, 620.
- Figura 4: Organtini LJ, Shingler KL, Ashley RE, Capaldi EA, Durrani K, Dryden KA, Makhov AM, Conway JF, Pizzorno MC, Hafenstein S. Honey Bee Deformed Wing Virus Structures Reveal that Conformational Changes Accompany Genome Release. J Virol. 2017 Jan 3;91(2):e01795-16.
- Figure 5 e 6: De Miranda, J. R., Gauthier, L., Ribiere, M., & Chen, Y. P. (2011). Honey bee viruses and their effect on bee and colony health. In Honey Bee Colony Health: Challenges and Sustainable Solutions (pp. 71–102).