Perché si usa?
Negli ultimi anni, é stato osservato un aumento della resistenza agli antibiotici da parte di batteri come Escherichia coli o Klebsiella pneumoniae, microorganismi coinvolti nella maggior parte delle infezioni nosocomiali e/o comunitarie.
In precedenti articoli, si é parlato del gruppo ESKAPE (acronimo di Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, Enterobacter spp), ovvero un gruppo di patogeni con un nome nome evocativo che ricorda la parola inglese “fuggire” e che fa riferimento alla capacità che questi hanno di evadere l’azione degli antibiotici.
Peró, uno degli aspetti più cruciali del fenomeno di antibiotico-resistenza é la capacitá che alcuni gram negativi, appartenenti alla famiglia delle Enterobacteriaceae, hanno sviluppato verso farmaci ad amplio spettro come i carbapenemici (imipenem, meropenem), utilizzati nel trattamento di infezioni gravi e spesso considerati come una “ultima spiaggia” nel caso di fallimento di altri composti.
Questo fenomeno, insieme alla mancanza di nuovi trattamenti, hanno stimolato la creazione di nuovi algoritmi terapeutici e di mezzi di coltura che aiutino a ottenere risultati nel minor tempo possibile e indirizzare cosí la terapia antibiotica. Esistono vari studi che hanno messo in luce l’importanza del diagnostico rapido, accompagnato da tecniche molecolari all’avanguardia (anche nello studio dell’evoluzione dei geni di resistenza). Nonostante tutto, la coltura dei campioni é il gold standard. Uno dei mezzi ampiamente utilizzati nel laboratorio di microbiologia clinica é il CHROMID® Carba, terreno solido selettivo e differenziale per l’identificazione di E. coli e K. pneumoniae produttori di carbapenemasi.
Composizione del terreno
Gli ingredienti base sono i seguenti:
- Peptone di carne (suino o bovino) 13 g
- Peptone di soia 5g
- Carboidrati 1g
- L-triptofano 0,9g
- Tampone fosfato 1g
- Miscela di nutrienti 2g
- Agar 18g
- Miscela selettiva 1,35g
- Miscela cromogenica 1,23g
- Acqua purificata 1L
Con un pH finale di 7,4. Si conserva a 2/8 °C, visto che viene giá fornito come terreno solido. É importante mantenerlo al buio, onde evitare la degradazione del reattivo cromogenico. Non é consigliato utilizzarlo se non mantenuto alle condizioni ottimali.
Risultati della crescita
Il terreno CHROMID® Carba é adatto per investigare la presenza di patogeni produttori di carbapenemici, che colonizzano il paziente. Si possono utilizzare i campioni rettali (tamponi), strisciandoli direttamente sull’agar senza necessitá di arricchire previamente la coltura in mezzo liquido. L’incubazione viene fatta a 37 ºC, per 18-24 ore.
Le colonie di E. coli produttore di carbapenemasi appaiono rosa-bordeaux, mentre quelle di K. pneumoniae blu-verde.
Dopo l’identificazione su CHROMID® Carba agar, é consigliato effettuare una sub-cultura e determinati test di sensibilitá agli antibiotici per confermare i risultati e fornire un diagnostico corretto.
Immagini

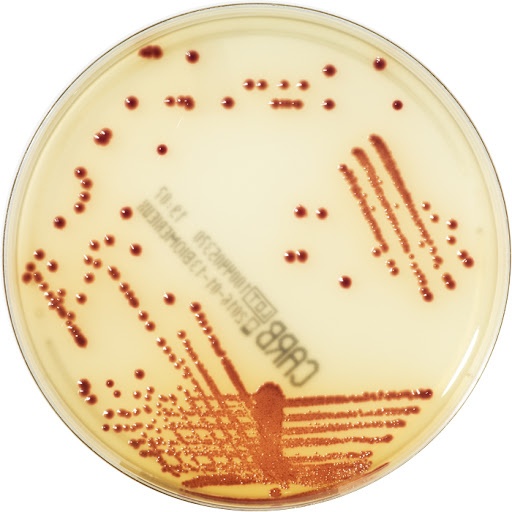

Limitazioni del terreno e validazione
Per validare il mezzo, sono stati utilizzati ceppi KPC (Klebsiella pneumoniae carbapenemase-producing) di K. pneumoniae ATCC® 1705™ e E. coli ATCC® 2340™, entrambi con espressione di geni di resistenza ai carbapenemici. Tali microorganismi, in coltura pura, sono stati testati per determinare il numero minimo di CFU/mL (colony forming units per millilitro) rilevate sull’agar CHROMID® CARBA. Dopo 18-24 ore di incubazione, la più bassa diluizione utile alla identificazione (limit of detection, LOD) di entrambi i ceppi é stata stabilita nel valore di 1,5×103 CFU/mL.
Sono stati effettuati test anche in colture miste, per validare la capacitá di identificare infezioni polimicrobiche dovute a microorganismi multiresistenti. Dopo 18-24 ore di incubazione, i risultati ottenuti hanno dimostrato che quando la concentrazione delle specie presenti non superava le 108 CFU/mL, si identificavano differenti colonie dei vari ceppi KPC che costituivano la miscela, con il caratteristico colore (rosa per l’E. coli o verde-azzurro per K. pneumoniae). Tuttavia, quando i vari ceppi sono presenti a concentrazioni maggiori di 108 CFU/mL, si possono verificare inibizioni reciproche.
Inoltre, la mancanza di crescita di colonie nel mezzo, non stabilisce la esatta negatività del campione.
Per maggiori informazioni, si puó fare riferimento al datasheet: https://www.accessdata.fda.gov/cdrh_docs/pdf18/K181092.pdf
Raffaella Onori, PhD
Fonti
- http://www.biomerieux-culturemedia.com/product/1-chromid-carba
- Onori, R., Gaiarsa, S., Comandatore, F., Pongolini, S., Brisse, S., Colombo, A., … & Bandi, C. (2015). Tracking nosocomial Klebsiella pneumoniae infections and outbreaks by whole-genome analysis: small-scale Italian scenario within a single hospital. Journal of clinical microbiology, 53(9), 2861-2868.
- Bouza, E., Onori, R., Semiglia-Chong, M. A., Álvarez-Uría, A., Alcalá, L., & Burillo, A. (2018). Fast track SSTI management program based on a rapid molecular test (GeneXpert® MRSA/SA SSTI) and antimicrobial stewardship. Journal of Microbiology, Immunology and Infection.