Principio
Virus come Orthomyxovirus, Paramyxovirus e Rubivirus, presentano delle glicoproteine superficiali, le emoagglutinine, capaci di legare i recettori dell’acido sialico sui globuli rossi provocandone così l’emoagglutinazione.
Quando le particelle virali si legano agli eritrociti, ne causano l’aggregazione formando in questo modo un reticolo di cellule. Se un virus emoagglutinante viene in contatto con un siero immune di un paziente che ha superato l’infezione o che è stato sottoposto a vaccinazione, perde la capacità di legarsi agli eritrociti perché viene sottratto dagli anticorpi specifici presenti. Quando il nostro organismo è esposto ad un virus, il sistema immunitario produce anticorpi specifici che innescano una risposta contro gli antigeni virali di superficie, inibendo così la loro azione.
Esistono alcuni test in grado di individuare le caratteristiche emoagglutinanti di un virus oppure la quantità di anticorpi prodotti contro di esso.
- Il Test di emoagglutinazione (HA), sviluppato negli anni 40, permette di identificare in maniera diretta la presenza di un virus emoagglutinante. Tale metodica è molto sfruttata per identificare la capacità di emoagglutinazione dei virus influenzali.
- Il Test di inibizione dell’emoagglutinazione (HI), una variante del test HA, è una metodica utilizzata per titolare il quantitativo di anticorpi specifici presenti nel siero di un paziente che ha contratto l’infezione virale. Questo test è inoltre ampiamente utilizzato per valutare la somiglianza antigenica tra i virus dell’influenza. Tale approccio è particolarmente utile per la selezione dei virus influenzali stagionali su cui lavorare per la produzione di un vaccino. I risultati del test HI possono dirci se gli anticorpi sviluppati dopo la vaccinazione sono protettivi contro il virus circolante; inoltre è possibile individuare i cambiamenti antigenici nei virus influenzali attualmente in circolazione rispetto a quelli diffusi in passato.
Metodo
Lo svolgimento dei test necessita di:
- Virus emoagglutinante;
- Anticorpi specifici in grado di inibire l’emoagglutinazione;
- Eritrociti emoagglutinabili specie-specifici in base alla tipologia di virus da individuare;
- Soluzione tamponata a ph ottimale per favorire la reazione;
- Soluzioni che inibiscono le emoagglutinine non specifiche presenti nel siero;
- Una piastra da microtiolazione da 96 pozzetti.
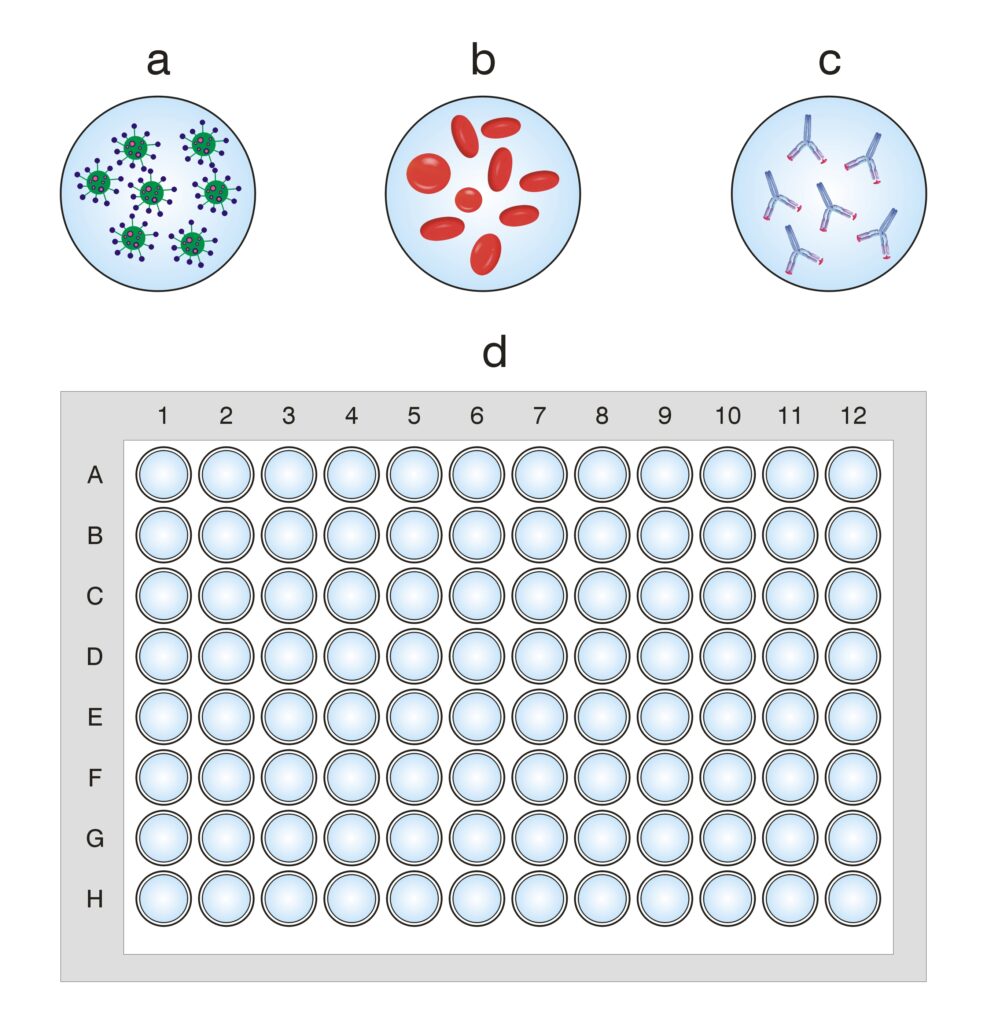
Procedura test di emoagglutinazione (HA)
Il test di emoagglutinazione per la titolazione virale prevede la distribuzione di una quantità standardizzata di globuli rossi all’interno di una piastra da microtitolazione da 96 pozzetti. In seguito, il virus in analisi è diluito in ogni rispettivo pozzetto. Le diluizioni della componente virale sono fondamentali per comprendere la capacità ed il grado di emoagglutinazione. Virus e globuli rossi sono incubati per 30 minuti a temperatura ambiente al fine di favorire la reazione di emoagglutinazione.
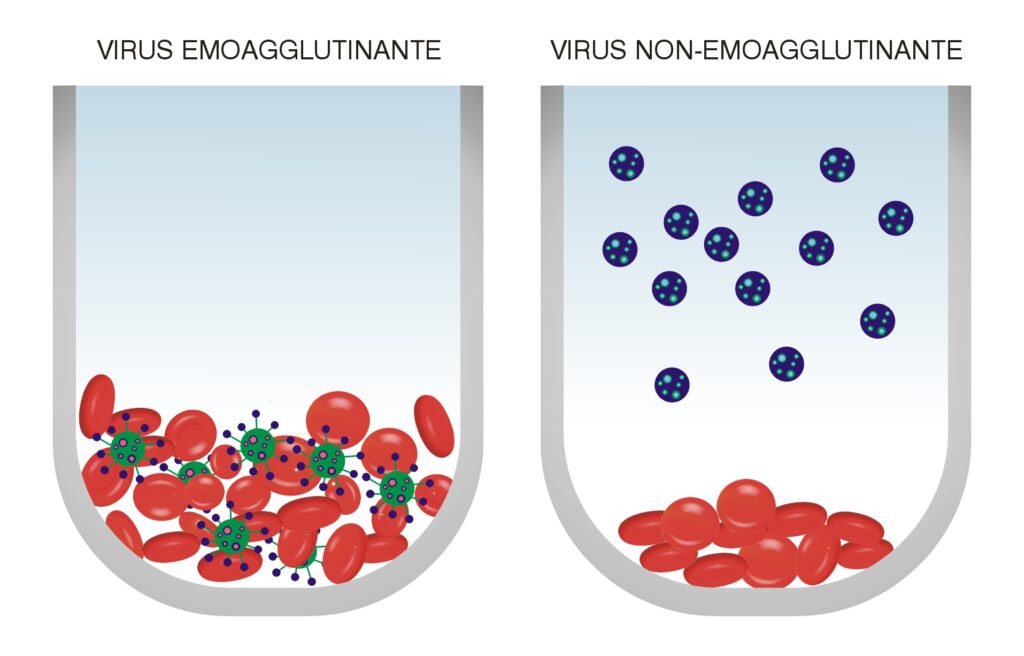
Se il virus presenta sulla propria superficie le emoagglutinine, provocherà l’aggregazione dei globuli rossi, impedendone così una normale precipitazione sul fondo del pozzetto. Al termine della procedura si prosegue con la lettura dei risultati.
Procedura test di inibizione dell’emoagglutinazione (HI)
Il test di inibizione dell’emoagglutinazione per la titolazione degli anticorpi prevede la diluizione del siero in esame e la sua incubazione in una piastra da 96 pozzetti dove è presente una quantità standardizzata di virus emoagglutiante. I pozzetti sono disposti secondo righe e colonne. Le file sono utilizzate per testare diversi virus influenzali contro lo stesso set di anticorpi, mentre le colonne evidenziano il numero di diluizioni del siero effettuate. La piastra è lasciata riposare a temperatura ambiente per circa 60 minuti al fine di favorire il legame degli anticorpi specifici con il virus, se presenti nel siero. In seguito, sono aggiunti i globuli rossi e si prosegue con l’incubazione per 30 minuti ad una temperatura di 4°C per far sì che si manifesti un’eventuale reazione di emoagglutinazione. Infine, si procede con la lettura dei risultati.

Risultati attesi
La presenza di una patina omogenea indica che si è verificata l’emoagglutinazione. In questo caso è possibile osservare una distribuzione irregolare dei globuli rossi alla base del pozzetto.
Se nel siero in esame sono presenti anticorpi contro il virus emoagglutinante ne inibiranno la sua azione. Quindi, nel momento in cui il virus sarà messo in contatto con i globuli rossi non provocherà la loro agglutinazione. In tal caso si riscontra la presenza di un bottone a margini netti sul fondo del pozzetto.
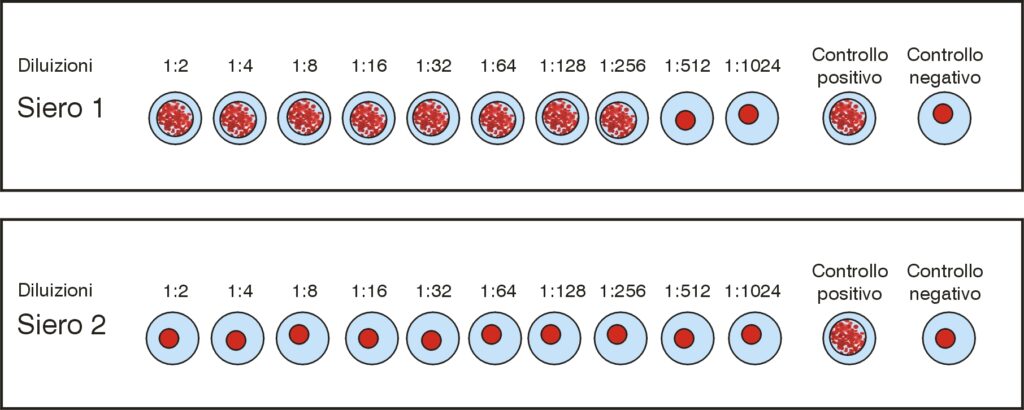
- Nel test di emoagglutinazione (HA), il titolo virale è valutato in base alla più elevata diluizione in cui si verifica emoagglutinazione. Ovvero, la più alta diluizione equivale al pozzetto in cui si può osservare ancora l’emoagglutinazione dei globuli rossi mediata dal virus.
- Nel test di inibizione dell’emoagglutinazione (HI), il titolo degli anticorpi in grado di inibire l’attività virale corrisponde alla più alta diluizione del siero in esame in cui si riscontra ancora un bottone a margini netti di globuli rossi alla base del pozzetto; cioè l’ultima diluizione in cui è presente un quantitativo sufficiente di anticorpi tale da inibire l’azione del virus.

Limitazioni del test
- Per ottenere una maggiore affidabilità dei risultati è necessario un accurato controllo dei tempi di incubazione, tipologia e concentrazione dei globuli rossi utilizzati.
- Fattori non specifici nel campione possono causare interferenze e valori di titolo errati. Ad esempio, molecole diverse dagli anticorpi specifici del virus nel campione possono inibire l’agglutinazione tra virus e globuli rossi, oltre a bloccare potenzialmente il legame dell’anticorpo con il virus.
- La valutazione dei risultati di HA e HI è affidata ad una persona qualificata nella lettura della piastra e nella determinazione dei valori del titolo. Il metodo di interpretazione manuale può favorire la possibilità di una lettura dei risultati errata.
Quality control
I campioni analizzati mediante il test HA sono sempre affiancati da:
- Controllo negativo: Pozzetto in cui è assente il virus;
- Controllo positivo: Pozzetto in cui è presente il virus emoagglutinante.
I vari campioni analizzati mediante il test HI sono sempre affiancati da:
- Controllo positivo: Siero noto contenente anticorpi specifici;
- Controllo negativo: Siero noto senza anticorpi specifici;
- Siero e cellule senza antigene per rilevare un’eventuale emoagglutinazione non specifica.
Fonti
https://www.who.int/csr/resources/publications/influenza/whocdscsrncs20025rev.pdf