Caratteristiche
Il verme Gastrodiscoides hominis (chiamato anche Gastrodiscus hominis o Amphistomun hominis) è un parassita intestinale che rientra nella classe dei Trematodi e nella sottoclasse dei Digenei (caratterizzati da due tipologie di riproduzione, sessuata e asessuata), e rappresenta l’unica specie del genere Gastrodiscoides. La scoperta e la descrizione di questo platelminta (verme piatto) risale al 1876, quando due medici britannici, Richard Lewis e James McConnell, lo individuarono nell’intestino cieco di un uomo, e diedero poi un’esposizione incompleta e inaccurata della struttura interna, affermando che il parassita possedeva un testicolo e un ovaio. Nel 1906 il parassitologo britannico John William Watson Stephens fornì una nuova relazione usando un campione prelevato da un abitante di Assam, una regione dell’India. Egli amplificò la rappresentazione del parassita e corresse alcune parti dell’asserzione di Lewis e McConnell, come ad esempio l’anatomia interna.
All’inizio questo platelminta venne inserito nel genere Amphistoma, nel 1902 il veterinario polacco Franz Fischoeder, notando l’affinità con altre specie, lo piazzò, in maniera provvisoria, nel genere Gastrodiscus; l’appartenenza a questo genere venne confermata nel 1906 da Stephens. Tuttavia, nel 1913 Robert Thomas Leiper, un elmintologo del London School of Tropical Medicine, riesaminò l’elminta e constatò la presenza di caratteri distintivi come un tubercolo genitale, la posizione dell’orifizio genitale, un disco ventrale liscio e i testicoli disposti in fila indiana. Tali proprietà lo indussero e creare il genere Gastrodiscoides. Tuttavia, questa classificazione incontrò diverse critiche che ne impedirono l’approvazione generale. Più tardi si osservò che il parassita era molto più ricorrente nei maiali e in altri mammiferi piuttosto che negli umani. La prima documentazione di infezione nei maiali apparve nel 1911 in Vietnam; nel 1913 venne confermato che il tasso di infezione suina raggiungeva il 5%. In seguito un gran numero di vermi intestinali fu recuperato dai traguli maggiori (Tragulus napu) morti nei Giardini Zoologici della Società di Zoologia di Londra. Questi animali provenivano da Malay (Francia) ed erano la collezione del principe del Galles. I limiti delle descrizioni di Leiper non prevennero il sostenimento crescente a favore del nome generico Gastrodiscoides nel precoce 1920.
La nomenclatura attualmente accettata fu rinforzata dal parassitologo britannico J. J. C. Buckley al London School of Hygiene and Tropical Medicine, le cui rappresentazioni si fondavano sull’alta incidenza dell’infezione tra i nativi di Assam nell’India nordorientale. Il suo primo resoconto del 1939, seguito da una serie di evidenze che supportavano la proposta di Leiper, difese la validità di un genere separato, Gastrodiscoides, e quindi del nome binomiale Gastrodiscoides hominis. Il suo rapporto raffigurò la descrizione pioniera del ciclo vitale del verme e la prevalenza delle gastrodiscoidiasi; nel suo sondaggio riguardante tre villaggi di Assam, si constatò che più del 40% della popolazione era infetta. La relazione di Buckley raffigura lo strumento più utile alla moderna classificazione del G. hominis.
Dal punto di vista morfologico il verme adulto appare di colore rosa acceso-rossastro (Fig. 1), misura 5-8 mm di lunghezza e 3-5 mm di larghezza. Il corpo è bilateralmente simmetrico, appiattito a livello dorsoventrale, e ricoperto da un tegumento con numerosi tubercoli; la regione anteriore è di forma conica, mentre quella posteriore è discoidale. Il canale alimentare è incompleto ed è composto da un paio di borse laterali, che si elevano dalla ventosa orale (situata nella regione anteriore), e un tubo faringeo che si biforca in due intestini ciechi, i quali, nella parte terminale, si inclinano leggermente verso l’interno e poggiano sulla ventosa ventrale (o acetabolo) retrostante la bocca. La ventosa orale è circondata da papille ciliate e non ciliate. La vescica escretoria si trova nel centro e dietro la ventosa ventrale (Fig. 1).
Come gli altri digenei, G. hominis è ermafrodita, ovvero possiede gli organi riproduttivi sia maschile che femminile posizionati nell’area posteriore. L’ovaio, avente una forma ovale, è collocato più o meno sulla linea media del corpo, più vicino alla superficie ventrale e posteriormente ai due testicoli; l’utero si trova postero-lateralmente a destra dell’ovaio e più vicino alla superficie dorsale, è vagamente a spirale e si apre sul poro genitale. I testicoli, adiacenti alla biforcazione intestinale, sono divisi in lobuli e adagiati l’uno sull’altro; nella parte dorsale di ognuno sono situati i vasi efferenti, che si uniscono in un vaso comune. Questo presenta una porzione dilatata, che forma una vescicola seminale. Il dotto si apre sulla sommità della papilla genitale al di sotto dell’apertura del dotto femminile.
G. hominis risiede soprattutto nel colon e nel cieco del maiale, che è l’ospite naturale, ma può infettare anche altri animali, tra cui il tragulo maggiore, il ratto delle risaie (Rattus brevicaudatus), il macaco rhesus (Macaca mulatta), l’orango e l‘essere umano. Quest’ultimo raffigura un ospite accidentale, nel quale il parassita provoca la malattia chiamata gastrodiscoidiasi, che è una zoonosi.

Filogenesi
Dominio Eukaryota
Regno Animalia
Phylum Platyhelminthes
Classe Trematodi
Ordine Plagiorchiida
Famiglia Paramphistomidae
Genere Gastrodiscoides
Specie G. hominis
Epidemiologia
Le nazioni in cui G. hominis è prevalente sono Bangladesh, Burma, Cina, Kazakistan, Filippine, Vietnam, Russia (Delta del Volga) e India. In quest’ultima ci sono regioni in cui la preponderanza del platelminta è ragguardevole, tra queste abbiamo Assam, Bengal, Bihar, Madhya Pradesh, Orissa (Odisha) e Uttar Pradesh (Fig. 2). Comunque, si sono verificati dei casi isolati in Nigeria; uno di questi riguarda una bambina di sette anni che lamentava sintomi come malnutrizione e anemia, e alla fine le fu diagnosticata l’infezione da Ascaris lumbricoides e G. hominis. Dopo una terapia adeguata, la ragazza guarì.
L’alta incidenza di alcune zone può essere connessa alle scarse norme igienico-sanitarie, per esempio le fattorie e i villaggi dove si impiega il “suolo notturno”, ovvero la raccolta di escrementi umani da pozzi neri, abitazioni private, gabinetti, latrine di pozzi, fosse settiche. Tali escrementi possono essere venduti come fertilizzanti.
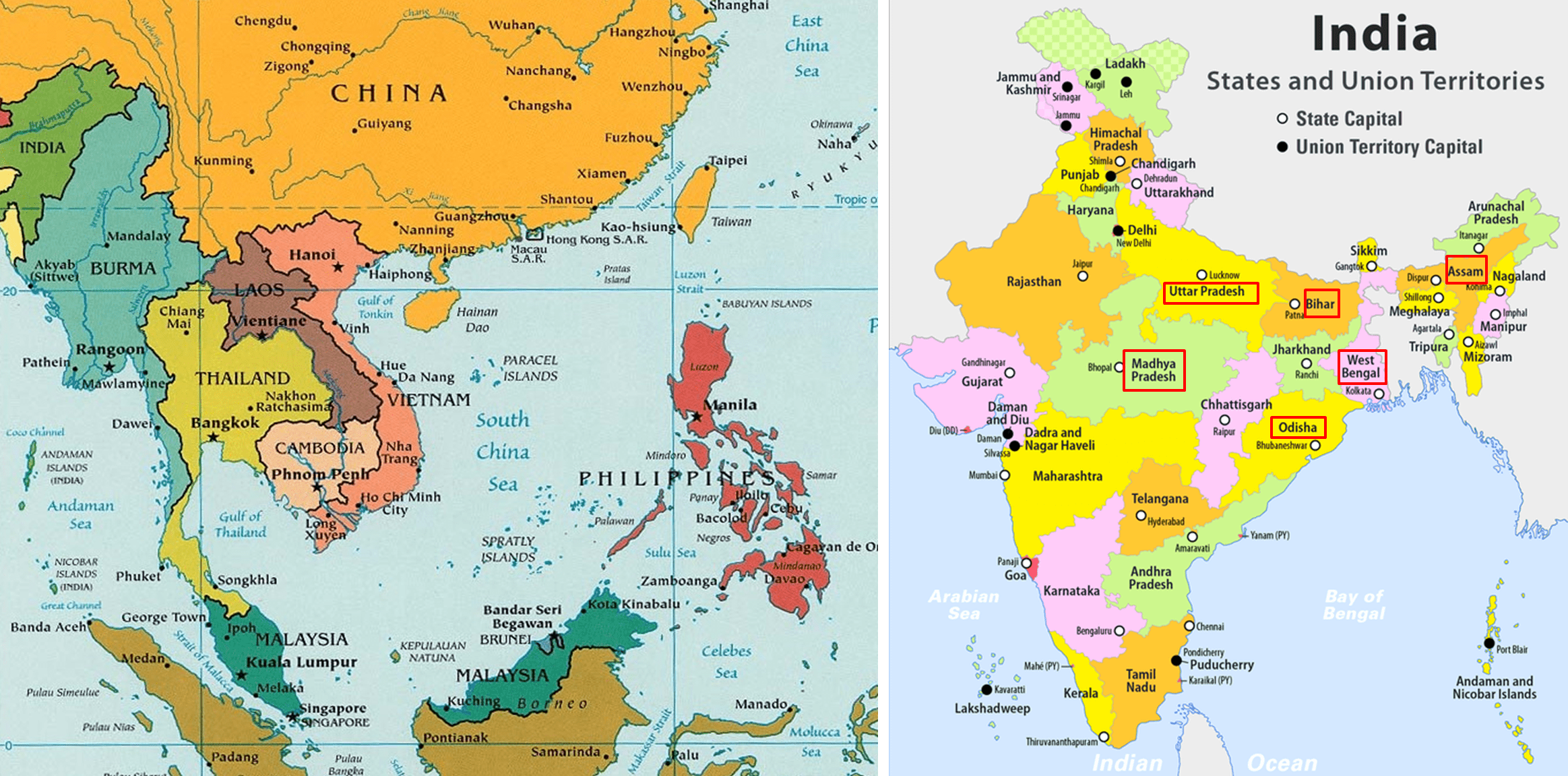
[Fonte: Stanford.edu / Wikipedia.org]
in India molti dati epidemiologici possono essere compresi prendendo in considerazione il fatto che G. hominis e Fasciolopsis buski utilizzano lo stesso mollusco come ospite intermedio. A Bereilly, il 27% dei 233 maiali portati al mattatoio erano infettati dl G. hominis, e nel 50% di questi casi tale infezione era concomitante con quella da F. buski.
Ciclo vitale e patogenesi
G. hominis è contraddistinto da un ciclo che implica la riproduzione asessuata in un mollusco gasteropode, che è l’ospite intermedio, e la riproduzione sessuata in un ospite vertebrato. Essendo ermafrodita, impiega l’autofecondazione al fine di depositare le uova, che sono di forma romboidale, trasparenti, verdastre-grigiastre e dotate di opercolo (organo mobile che chiude l’apertura da cui viene rilasciata la larva). Sono notevolmente simili a quelle di Fasciolopsis buski e di Fasciola hepatica, ma poco più grandi (130-160 μm vs 130-150 x 60-90 μm); ognuna di esse contiene 24 cellule vitelline e un ovulo centrale non embrionato.

Nell’ambiente acquatico le uova si schiudono ed espellono il miracidio (il primo stadio larvale) nel giro di 9-14 giorni a una temperatura di 24-33° C; temperature più alte sono dannose per il suo sviluppo. Una volta libero nell’acqua, il miracidio infetta un mollusco gasteropode (il più comune è Helicorbis coenosus, che si trova abbondantemente nei porcili), all’interno del quale raggiunge lo stadio di sporociste, seguito dalla fase di redia e infine di cercaria. Le cercarie infettive vengono rilasciate sulle piante acquatiche, dove si sviluppano in metacercarie. Poiché è capitato di trovare pesci e altri animali acquatici infettati dal parassita, si è ipotizzato che le cercarie siano in grado di penetrare accidentalmente in altri animali acquatici, che si comportano come secondi ospiti intermedi, e diventare metacercarie. Gli ospiti definitivi, di cui fa parte anche l’essere umano, possono entrare in contatto con il parassita in seguito a ingestione di piante contaminate o pesce crudo infetto. A questo punto la metacercaria viaggia attraverso il tratto digerente fino ad arrivare al duodeno, dopodiché prosegue fino all’intestino cieco, dove si autofeconda e produce le uova, che vengono evacuate con le feci, consentendo al ciclo di ricominciare (Fig. 4).

Negli esseri umani la gastrodiscoidiasi di solito è asintomatica, anche se ci sono situazioni in cui può manifestarsi con sintomi come diarrea, febbre, anemia, dolore addominale, coliche e un aumento della secrezione di muco. Nei casi più gravi, quando il verme adulto produce una grossa mole di uova, si possono verificare reazioni tissutali che colpiscono il cuore o i vasi linfatici mesenterici. Se la malattia non viene curata, può portare alla morte. In Thailandia ci fu un caso di una ragazza di 17 anni che era stata ricoverata presso l’ospedale di Bhudhachinaraj, nella provincia di Phitsanulok, la giovane in particolare lamentava la presenza di feci nelle urine da 15 giorni e, il giorno prima del ricovero, anche di molti vermi. Otto mesi prima della comparsa di questi sintomi, aveva avuto una storia di debolezza, anemia, perdita di peso, edema generale con una massa palpabile nella zona sovrapubica. Il giorno del ricovero la paziente era emaciata e anemica (emoglobina 6 mg/dl), manifestava edema della faccia e delle gambe, febbre e leucocitosi, senza eosinofilia. Dall’esame delle urine si individuò la presenza di globuli rossi e globuli bianchi, cilindri granulosi e albumina. Tuttavia, non venne trovato alcun parassita. L’analisi ai raggi X rivelò una fistola che collegava il digiuno alla vescica; questa venne corretta mediante chirurgia, ma la ragazza morì dopo l’operazione. L’autopsia confermò la presenza della fistola e in aggiunta a ciò svelò linfosarcoma dell’intestino crasso e dei linfonodi mesenterici.
Nei maiali, invece, i sintomi patologici della gastrodiscoidiasi sono l’infiltrazione dei granulociti eosinofili, dei linfociti e delle plasmacellule indotta dall’attaccamento dei parassiti alla mucosa. Ciò conduce a un’infiltrazione anche della sottomucosa, che va incontro a edema e ispessimento, risultando in un’infiammazione subacuta dell’intestino cieco e diarrea mucoide. All’esame istopatologico si osservano la desquamazione marcata dell’epitelio, l’ipersecrezione di muco e la necrosi delle ghiandole mucipare. La lamina propria (strato di tessuto connettivo lasso che si trova sotto l’epitelio delle mucose) è colpita da una massiva infiltrazione di eosinofili che si insinuano tra le cripte di Lieberkühn (ghiandole presenti nella lamina propria dell’epitelio dell’intestino tenue e dell’intestino crasso) insieme a linfociti, macrofagi e plasmacellule. La penetrazione di queste cellule immunitarie provoca l’ingrossamento della muscolaris mucosae (sottile strato di tessuto muscolare liscio che segna il limite della mucosa). Le mucose appaiono iperemiche e alcuni vasi sanguigni presentano infittimento della tonaca intima e invasione da parte di eosinofili e linfociti. In ogni caso, un quadro simile si può riscontrare anche nelle persone.
Sfortunatamente immagini dell’istopatologia della gastrodiscoidiasi non sono disponibili, ma per consentire ai lettori di avere una visione più chiara, inseriamo un’immagine dell’anatomia microscopica della mucosa intestinale dove sono indicati i vari costituenti, alcuni di essi citati nel testo (Fig. 5).
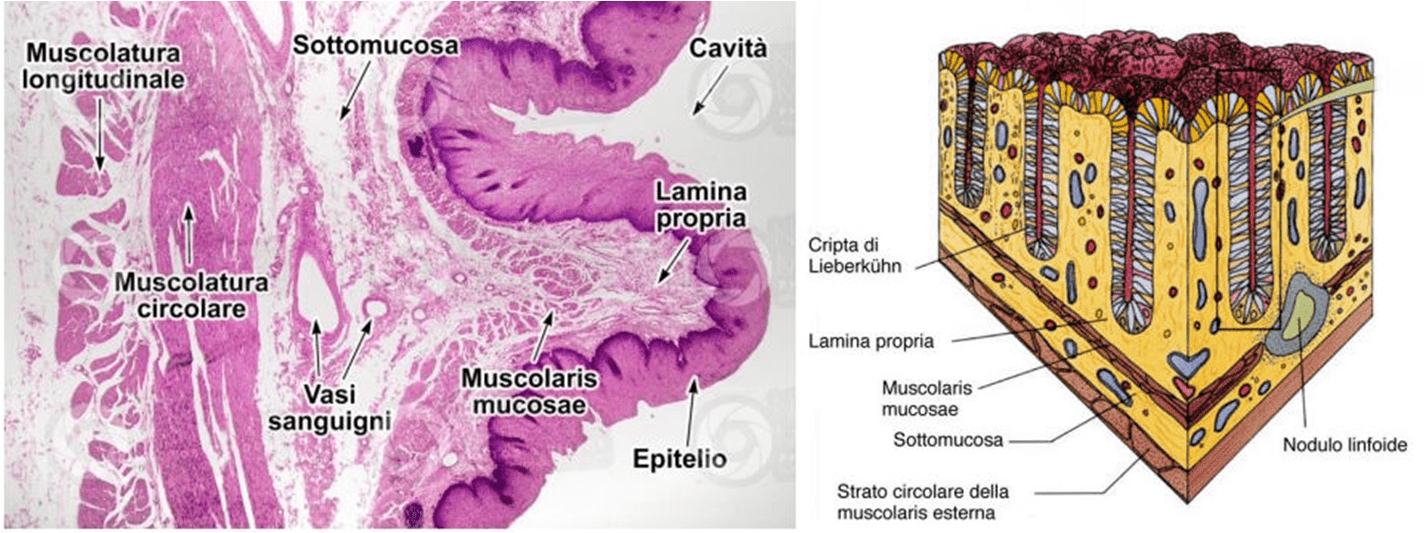
[Fonte: Uniba.it / Gastroepato.it]
Metodi di identificazione
La diagnosi di gastrodiscoidiasi consiste nella ricerca delle uova nelle feci. È importante discernere la gastrodiscoidiasi dalla fasciolopsiasi, in quanto entrambi i nematodi si sovrappongono in molte aree endemiche dell’Asia. Le uova di G. hominis sono facilmente distinguibile da quelle di F. buski, in quanto queste ultime sono ovali e giallognole-marroni (Fig. 6). Il verme adulto è inconfondibile in seguito a espulsione spontanea o dopo trattamento con clisteri a base di acqua e sapone o con antielmintici.
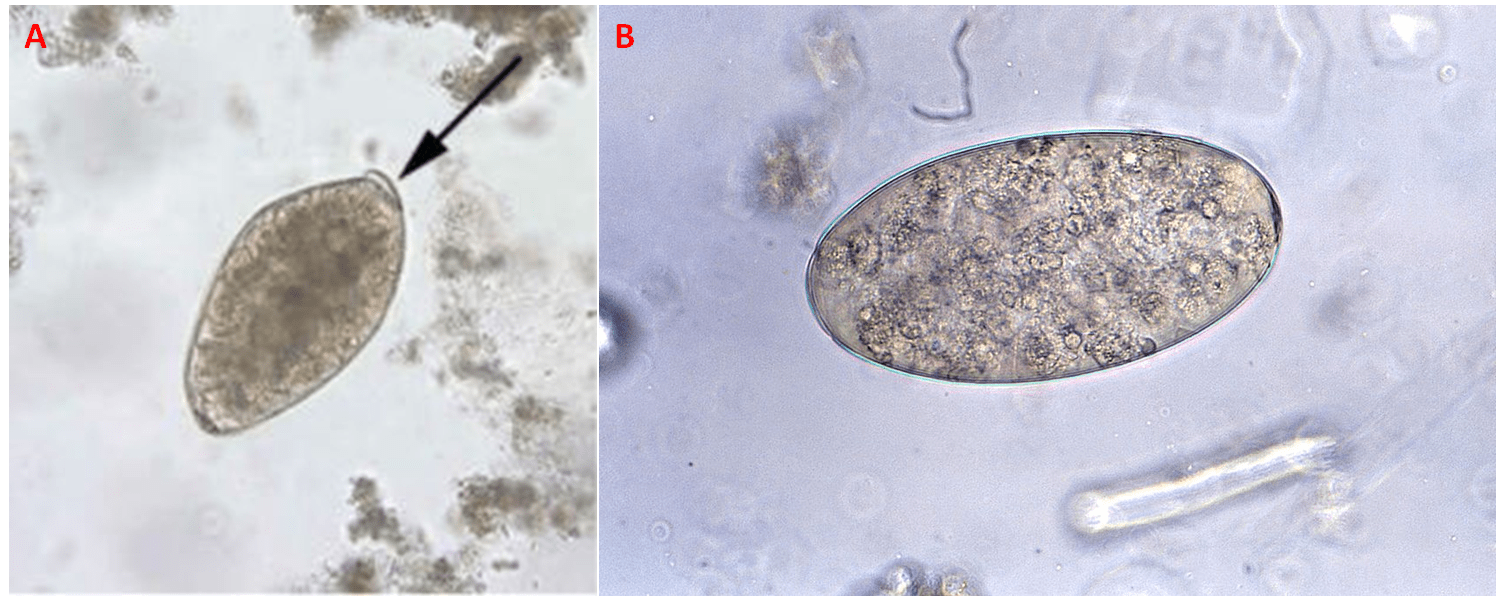
Dal momento che l’identificazione morfologica non è sempre univoca, sono alquanto diffuse le metodiche basate sull’analisi del DNA, ovvero PCR (reazione a catena della DNA polimerasi) e sequenziamento, che permettono di risolvere i problemi tassonomici in maniera accurata. A tal proposito si possono utilizzare le sequenze di DNA non codificanti ITS1 e ITS2 (sequenza di DNA spaziatore interna di tipo 1 e 2). In uno studio del 2009, pubblicato su Parasitology Research, un gruppo di ricercatori isolò il DNA da vermi adulti e uova derivanti dall’intestino di maiali ad Assam e a Meghalaya, per poi amplificare le sequenze ITS usando due coppie di oligonucleotidi universali basati sulle sequenze ITS delle specie di Schistosoma: BD1 e 4S per ITS1 e 3S e A28 per ITS2. Le dimensioni delle due sequenze erano 841 pb e 494 pb rispettivamente, e l’allineamento tra le sequenze ITS2 del DNA estratto dalle uova e di quello proveniente dagli adulti si rivelarono considerevolmente simili, e ciò testimoniò l’assenza di differenze frase specifiche (Fig. 7).

In seguito fu eseguita un’analisi bioinformatica mediante BLAST e si constatò che le sequenze generate dai campioni delle due aree geografiche erano identiche. Le analisi filogenetiche delle sequenze ITS1 e 2 dimostrarono che G. hominis presenta una stretta somiglianza con i membri delle famiglie Paramphistomidae, Echinostomatidae e Fasciolidae.
Questo lavoro raffigura la prima caratterizzazione molecolare di G. hominis basata sulle sequenze ITS1 e ITS2. Tuttavia, al fine di accertare le variazioni intra-specie dei ceppi e determinare la variabilità genetica e strutturale della popolazione, è opportuno studiare gli isolati G. hominis provenienti da diverse zone della regione usando dei marcatori molecolari aggiuntivi.
Terapia e prevenzione
Per la gastrodiscoidiasi non esiste uno specifico trattamento, anche se la tradizionale procedura dei clisteri a base di sapone è efficace nel rimuovere i vermi adulti dal colon. Alcuni farmaci che si sono dimostrati validi sono il tetracloroetilene con un dosaggio di 0,1 mg/kg somministrato a stomaco vuoto, e ancora più preferibile è il Praziquantel (Biltricide) impiegato anche nella paragonimiasi, di cui sono sufficienti tre dosi da 25 mg/kg, somministrate in un unico giorno, per eliminare il parassita. Questo farmaco agisce inducendo la vacuolizzazione del tegumento del verme, guastandone l’integrità. Non è dannoso per il feto, quindi può essere preso anche in gravidanza, tuttavia è controindicato durante l’allattamento, poiché compare nel latte materno. Una bambina nigeriana di sette anni (di cui abbiamo accennato nella parte sull’epidemiologia) è stata curata con il Mebendazolo (Vermox) che, a una singola dose di 500 mg, si è rivelato efficiente. Questo farmaco si attacca alla tubulina del parassita bloccando la generazione dei microtubuli, importanti per la divisione cellulare. Esso esibisce una potente attività verso svariati tipi di vermi parassiti intestinali, tra cui Enterobius vermicularis, Ascaris lumbricoides, Trichuris trichiura, Ancylostoma duodenale, Necator americanus, Strongyloides stercoralis, Taenia spp.
Per quanto concerne la profilassi, è fondamentale applicare semplici norme sanitarie, per esempio evitare l’impiego del “suolo notturno” come fertilizzante, lavare accuratamente le verdure, cuocere bene la carne e mettere in pratica tecniche adeguate per lo smaltimento dei rifiuti. In aggiunta a ciò, se si individua la presenza di G. hominis nelle feci dei maiali, bisogna sottoporli a trattamento farmacologico. Nelle aree endemiche la migliore misura per controllare l’infezione negli ospiti abituali del verme (i maiali) è quella di modernizzare gli allevamenti suini.
Fonti
- L. M. Goswami, P. K. Prasad, V. Tandon and A. Chatterjee. 2009. “Molecular characterization of Gastrodiscoides hominis (Platyhelminthes: Trematoda: Digenea) inferred from ITS rDNA sequence analysis”, Parasitology Research
- M. Khalil. 2016. “A Description of Gastrodiscoides hominis from the Napu Mouse Deer”, Proceedings of the Royal Society of Medicine
- Buckley J. J. C. 1939. “Observations on Gastrodiscoides hominis and Fasciolopsis in Assam”, Journal of Helminthology
- Mas-Coma S., Bargues M. D., Valero M. A. 2006. “Gastrodiscoidiasis, a plant-borne zoonotic disease caused by the intestinal amphistome fluke Gastrodiscoides hominis (Trematoda: Gastrodiscidae)”, Revista Ibérica de Parasitología
- Kumar V. 1980. “The digenetic trematodes, Fasciolopsis buski, Gastrodiscoides hominis and Artyfechinostomum malayanum, as zoonotic infections in South Asian countries”, Ann Soc Belg Med Trop
- Dada-Adegbola H.O., Falade C.O., Oluwatoba O.A., Abiodun O.O. 2004. “Gastrodiscoides hominis infection in a Nigerian-case report”, West African Journal of Medicine.
- Murty C.V., Reddy C.R. 1980. “A case report of Gastrodiscoides hominis infestation”, Indian J Pathol Microbiol.
- Liu D. 2012. “Molecular Detection of Human Parasitic Pathogens”, Boca Raton, FL: CRC Press
- Tandon V., Maitra S.C. 1983. “Surface morphology of Gastrodiscoides hominis as revealed by scanning electron microscopy”, Journal of Helminthology
- Baker D.G. 2008. Flynn’s Parasites of Laboratory Animals (2 ed.), Blackwell Publishers
- Brennan G.P., Hanna R.E., Nizami W.A. 1991. “Ultrastructural and histochemical observations on the tegument of Gastrodiscoides hominis“, International Journal for Parasitology
- Buckley J. J. C. 1964. “The problem of Gastrodiscoides hominis“, Journal of Helminthology
Fonti immagini: - http://www.ospedalebambinogesu.it/mebendazolo#.X9XhNVVKjIU
- https://web.stanford.edu/group/parasites/ParaSites2006/Gastrodiscoidiasis/gastro.htm
- https://it.wikipedia.org/wiki/Stati_federati_e_territori_dell%27India
- https://link.springer.com/chapter/10.1007%2F978-94-017-3594-0_7
- https://slideplayer.com/slide/17943275/
- https://www.cdc.gov/dpdx/fasciolopsiasis/index.html
- https://it.wikipedia.org/wiki/Fasciolopsis_buski#/media/File:Fasciolopsis_buski_egg_08G0039_lores.jpg
- https://www.uniba.it/docenti/coluccia-mauro/attivita-didattica/materiale-didattico/7-patologia-app-digerente.pdf
- https://www.gastroepato.it/coliti.htm
- https://www.albanesi.it/alimentazione/cibi/maiale.htm