Caratteristiche
La malattia da Herpesvirus delle Carpe Koi (Koi Herpesvirus Disease, KHVD) è una malattia acuta, altamente contagiosa e colpisce diversi organi e tessuti. Questa scheda virologica introduce Koi Herpesvirus e propone degli approfondimenti sui metodi di identificazione, sulla patogenesi e sugli eventuali trattamenti. La malattia qui descritta è stata osservata solamente nella specie Cyprinus carpio, ossia la Carpa comune, in tutte le sue varianti fenotipiche (carpa regina, carpa specchio e carpa cuoio) comprese le variopinte carpe koi. I primi episodi documentati di malattia da Herpesvirus delle Carpe Koi risalgono al 1997-98, quando diverse pubblicazioni descrissero la presenza della malattia negli Stati Uniti, nello stato di Israele e in Europa, dove però successive indagini retrospettive indicarono che il virus era già presente nel 1996.
Questa malattia colpisce esemplari di tutte le età con un tasso di mortalità superiore al 90% e perfino maggiore nei soggetti più giovani. La trasmissione del virus può avvenire principalmente attraverso l’acqua o il contatto con un esemplare infetto di carpa oppure con un pesce di un’altra specie in cui l’infezione è asintomatica, come nei carassi, nelle tinche, nelle carpe erbivore, nei pesci gatto, nei lucci e nelle trote.
In pochi anni Koi Herpesvirus (KHV) si è diffuso tra le popolazioni di carpe, soprattutto in quelle allevate, e attualmente questo agente infettivo ha una distribuzione geografica su scala mondiale, se si esclude l’Australia. Il motivo della rapida diffusione del virus è stato attribuito al commercio e alla movimentazione di esemplari vivi infetti, ma apparentemente sani. Infatti, i soggetti che sopravvivono all’infezione possono diventare dei portatori sani e continuare a contagiare gli altri esemplari per il resto della loro vita, e le carpe koi hanno una vita decisamente lunga.
Filogenesi
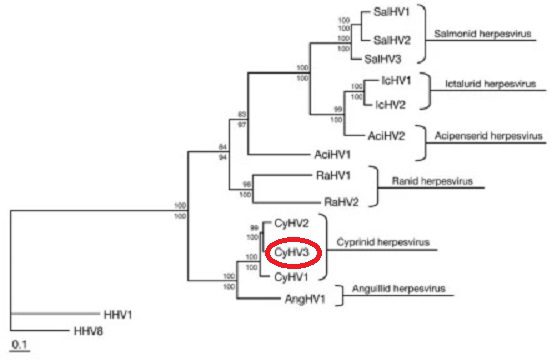
La presente scheda virologica illustra la classificazione di Koi Herpesvirus e come approfondimento è indicata la sua posizione rispetto agli altri membri della famiglia Alloherpesviridae.
| Dominio | Virus |
| Clade | Duplodnaviria (Virus a dsDNA) |
| Regno | Heunggongvirae |
| Phylum | Peploviricota |
| Classe | Herviviricetes |
| Ordine | Herpesvirales |
| Famiglia | Alloherpesviridae |
| Genere | Cyvirus |
| Specie | Cyvirus cyprinidallo3 |
| Sottospecie | Cyprinid herpesvirus 3 |
Genoma
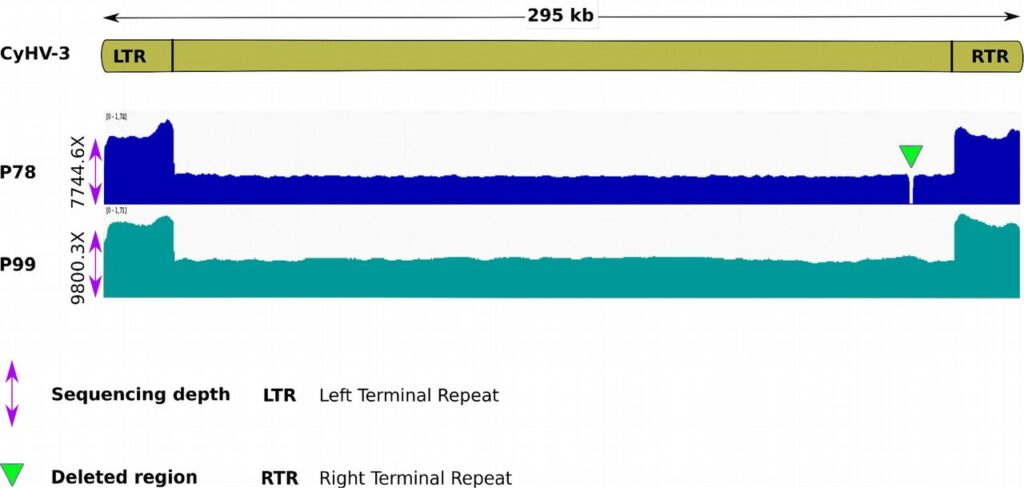
[Fonte: Fuandila et al., 2022].
Il genoma è costituito da una molecola lineare di DNA a doppio filamento lunga 295mila paia di basi. Le due estremità di questa molecola sono formate da sequenze ripetute e sono chiamate Left Repeat region e Right Repeat region. Questo genoma è stato descritto nel 2007, come formato da 156 geni codificanti per proteine, la maggior parte dei quali è comune a tutti gli Herpesvirus. Alcune ricerche svolte successivamente sulle sequenze di KHV provenienti da tre diverse aree geografiche, Stati Uniti, Israele e Giappone, hanno evidenziato un grado di somiglianza dei rispettivi genomi superiore al 99%.
Immagini al microscopio
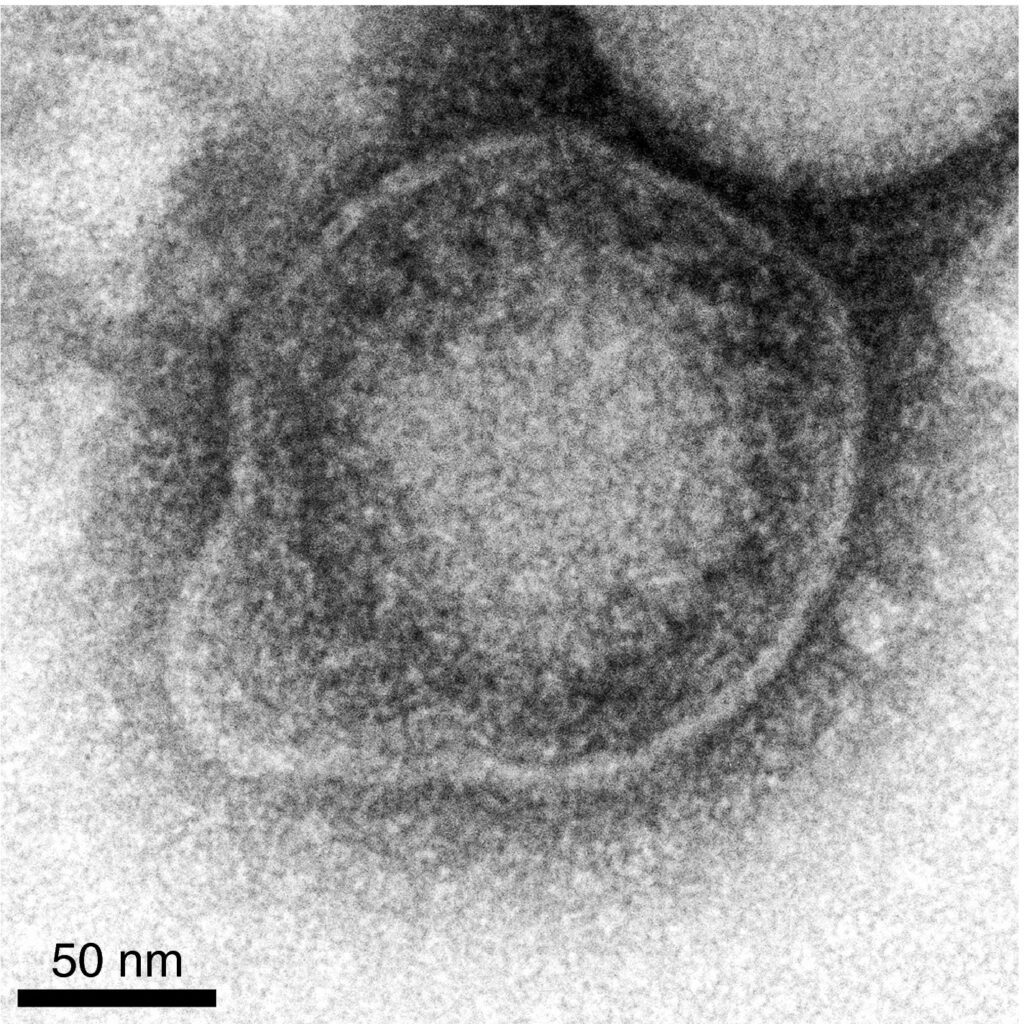
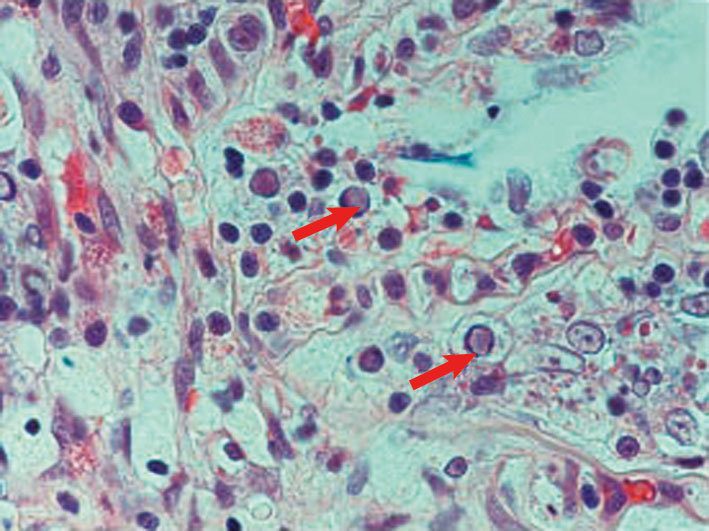
Struttura virale
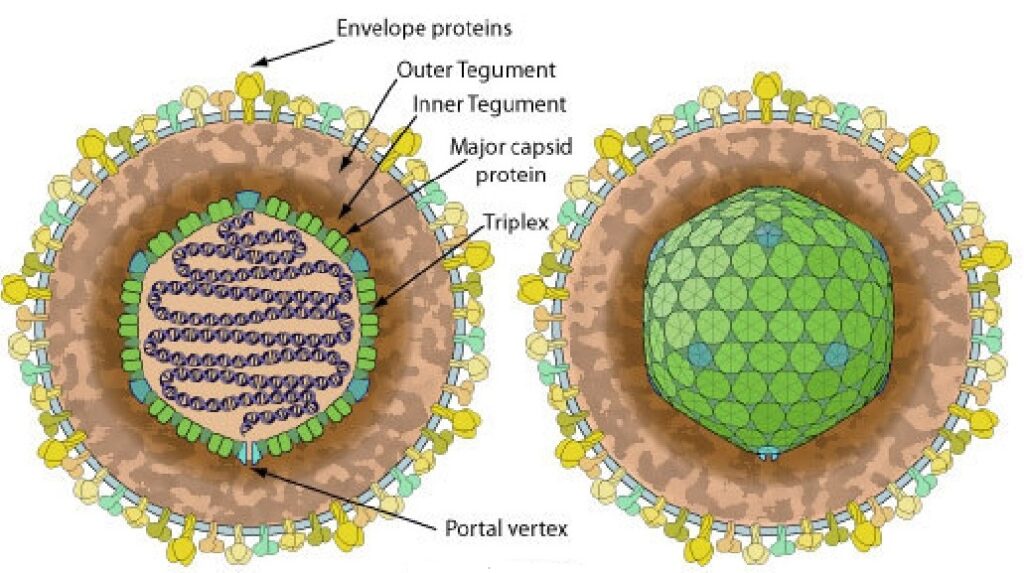
Il DNA virale è racchiuso all’interno di un capside formato da proteine, dal diametro di 100-110 nm, il quale ha la forma di un icosaedro, una figura geometrica solida con 20 facce triangolari uguali tra loro. Il capside è circondato da un successivo strato chiamato tegumento che a sua volta è contenuto dall’envelope, una membrana di fosfolipidi e proteine, il diametro complessivo del virione raggiunge dimensioni comprese tra i 170-230 nm a seconda del tipo di cellula infettata. Ogni particella virale comprende 40 proteine virali e 18 proteine dell’ospite.
Gli approfondimenti alla presente scheda virologica relativa a Koi Herpesvirus propongono: i metodi diagnostici, la patogenesi e i trattamenti.
Metodi di identificazione
Nei casi in cui si sospetta un’infezione da KHV la tecnica più utilizzata al fine di eseguire una diagnosi di conferma è la PCR (reazione a catena della polimerasi). Questa tecnica permette di ottenere numerose copie di una specifica porzione di DNA, in questo caso DNA virale. I campioni da testare possono provenire da soggetti morti e in lieve decomposizione, da soggetti asintomatici o da pesce congelato. In pratica, si prelevano piccoli pezzetti di branchia o di rene, che sono conservati in alcol etilico. Da questi campioni si estrae il DNA, il quale funziona come uno stampo sul quale si effettua la PCR. Successivamente questo DNA può essere sequenziato per conoscere la successione delle basi azotate che lo compongono e poterla confrontare con sequenze provenienti da virus della stessa specie già registrate in apposite banche dati.
Altri metodi meno utilizzati, ma dotati di buona sensibilità e specificità si basano
- sulla ricerca degli antigeni virali (immunofluorescenza, immunoistochimica, test ELISA);
- sulla ricerca dell’RNA di origine virale (ibridazione in situ).
In alcuni casi per la diagnosi di conferma, si possono utilizzare l’esame istopatologico o la microscopia elettronica, invece si sconsigliano l’analisi dei segni macroscopici, la microscopia ottica, l’isolamento in colture cellulari e la ricerca degli anticorpi contro il virus. Comunque, per avere la conferma di un’infezione da KHV ci si deve basare sulla positività ad almeno 2 o 3 test indipendenti.
Patogenesi
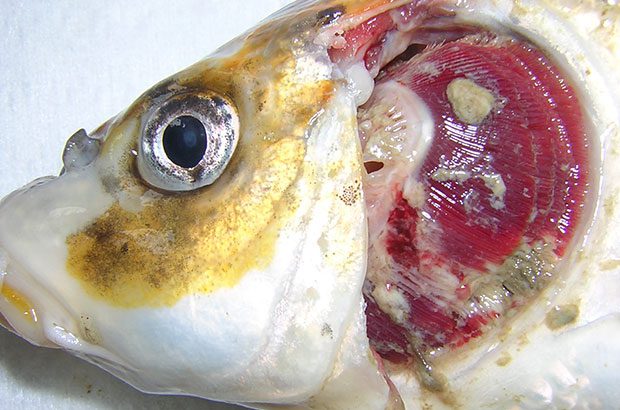
La malattia da Herpesvirus della carpa koi è caratterizzata da segni clinici comportamentali come sonnolenza e rifiuto del cibo, osservabili da 3 a 9 giorni dopo l’infezione, seguiti da un’elevata secrezione di muco dalla cute e dalle branchie, con evidenti difficoltà respiratorie. Inoltre, frequentemente si osserva enoftalmo, cioè l’occhio infossato. In pochi giorni dall’infezione il virus viene trasportato dai globuli bianchi e la malattia coinvolge gli organi interni, come il rene, la milza, il fegato e l’intestino. Successivamente sulle branchie si osservano proliferazioni, degenerazioni e lesioni dovute alla morte cellulare, mentre la cute, il rene e la milza presentano a loro volta degenerazioni cellulari. Comunque questi effetti compaiono in modo variabile, a seconda della virulenza del virus, della sua concentrazione, delle condizioni ambientali, in particolare della temperatura, e a seconda del pesce ospite.
L’assemblaggio delle particelle virali all’interno delle cellule avviene esattamente come osservato per gli altri Herpesvirus. Dapprima nel nucleo della cellula le proteine del capside si uniscono al DNA virale, successivamente il virione “matura” nel citoplasma. I soggetti infetti rilasciano particelle virali attraverso le feci, le urine e il muco. Gli esemplari che sopravvivono e guariscono dalla malattia dopo 64 giorni dall’infezione continuano ad incubare il virus nelle branchie e nel rene, e nonostante appaiano sani possono subire riattivazioni periodiche della malattia alternate a fasi di latenza per tutta la loro vita.
Terapia
Contro la malattia da KHV non esiste alcuna cura efficace. Tuttavia il virus può essere inattivato aumentando la temperatura dell’acqua fino a oltre 30°C. La sopravvivenza delle carpe può essere favorita dalla buona qualità dell’acqua, dall’adeguata presenza di ossigeno disciolto e dai trattamenti con antibiotici, utili al fine di curare le infezioni batteriche secondarie. Gli esemplari che sopravvivono all’infezione e al trattamento potrebbero comunque diventare dei portatori sani del virus, con il rischio di propagare la malattia. Recenti esperimenti indicano che l’inibitore delle istone demetilasi ML324 sarebbe un buon candidato come farmaco antivirale.
Applicazioni biotecnologiche
Molti gruppi di ricerca, in tutto il mondo, stanno studiando KHV allo scopo di produrre vaccini, che proteggano i pesci da questo agente infettivo. Per fare ciò, occorre definire:
- a) la natura del vaccino
- inattivato,
- vivo attenuato,
- a DNA;
- b) la modalità di somministrazione
- per immersione,
- per iniezione,
- per via orale.
I vaccini vivi attenuati, venduti in Israele, si ottengono attraverso ripetute replicazioni del virus in colture cellulari e mediante radiazioni ultraviolette. La somministrazione avviene per immersione o per iniezione: il virus vaccinale infetta solo la specie Cyprinus carpio, e non viene rilasciato dagli esemplari infetti. I produttori di questo vaccino dichiarano che esso conferisce una protezione superiore all’80%. In Germania e in Indonesia sono stati prodotti dei vaccini inattivati, mentre i vaccini a DNA sono ancora in fase sperimentale. Per ulteriori approfondimenti alla presente scheda virologica dedicata a Koi Herpesvirus si raccomandano i testi qui di seguito citati.
Fonti
- Patrick T.K. Woo, David W. Bruno. Fish Deseases and Disorders Volume 3: Viral, Bacterial and Fungal Infections – 2nd Edition, 2011. CABI. ISBN 978-1-84593-554-2.
- John A. Plumb, Larry A. Hanson. Health Maintenance and Principal Microbial Diseases of Cultured Fishes -Third Edition, 2011. Wiley-Blackwell. ISBN 9780470958353.
- Ronald J. Roberts. Fish Pathology – 4th Edition, 2012. Wiley-Blackwell. ISBN 9781118222942.
- Bergmann SM, Jin Y, Franzke K, Grunow B, Wang Q, Klafack S. Koi herpesvirus (KHV) and KHV disease (KHVD) – a recently updated overview. J. Appl. Microbiol. 2020;129(1):98-103.
- World Organisation for Animal Health (OIE). Manual of Diagnostic Tests for Aquatic Animals – 8th Edition, 2021. ISBN 978-92-95115-59-0.
Crediti immagini
- Immagine in evidenza: https://www.kodamakoisupply.com/wp-content/uploads/2022/07/koi-food-choose.jpg
- Figura 1: https://media.springernature.com/lw685/springer-static/image/art%3A10.1186%2F1297-9716-44-85/MediaObjects/13567_2013_Article_454_Fig1_HTML.jpg?as=webp
- Figura 2: https://www.biorxiv.org/content/biorxiv/early/2022/03/10/2022.03.10.483410/F1.large.jpg
- Figura 3: https://ami-journals.onlinelibrary.wiley.com/cms/asset/7cbdd879-47e4-4af2-b2dd-9b20a9bfe692/jam14616-fig-0001-m.jpg
- Figura 4: https://www.researchgate.net/profile/Michael-Gotesman/publication/250924475/figure/fig3/AS:601648015618048@1520455473160/Cyprinus-carpio-Koi-herpesvirus-forming-inclusion-bodies-arrows-in-gill-epithelium-of.png
- Figura 5: https://www.semanticscholar.org/paper/An-investigation-into-the-existence-of-cyprinid-Donohoe/e2223c2b733702e88b02e3f4a64b946214993cda/figure/0
- Figura 6: https://marinescience.blog.gov.uk/wp-content/uploads/sites/38/2016/07/KHV-Gill-Necrosis.jpg
Buon giorno Shascha mi potrebbe dire chi è il produttore di vaccini vivi attenuati contro l’herpes virus in Israle?
grata fin d’ora epr il suo aiuto
saluti
Anna Romagnolo Regusini
e mail anna_romagnolo@yahoo.it
La ditta Israeliana si chiama KoVax e detiene il brevetto per quel vaccino.