La biologia biomedica promuove l’innovazione nella ricerca biomedica e nell’industria farmaceutica, perché comprende diversi settori, interconnessi fra loro.
Definizione di biologia biomedica
La biologia biomedica è una scienza multidisciplinare che utilizza organismi, sistemi o processi biologici per sviluppare tecnologie e prodotti a beneficio della salute umana. La biologia biomedica comprende varie discipline, fra le quali: genetica, microbiologia, immunologia, biologia cellulare, biochimica, farmacologia e biologia del cancro.
Storia della biologia biomedica
Il rapporto tra la medicina e lo studio della vita è antico quanto la medicina stessa. Tuttavia, gli storici hanno evidenziato la grande trasformazione avvenuta nel XIX secolo, quando prima la fisiologia e poi la microbiologia divennero risorse importanti per la classificazione, la diagnosi e il trattamento delle malattie umane.
La scoperta del DNA
La biologia biomedica è nata dopo il 1945, con le scoperte sulle strutture macromolecolari, in particolare DNA e geni.
La struttura dell’acido desossiribonucleico (DNA), oggi nota come “doppia elica”, è stata scoperta nel 1953 da James Watson e Francis Crick. Questa è stata una delle pietre miliari che hanno definito la genetica, come la conosciamo oggi, ed è stata la spina dorsale di ricerche successive che provengono dal mondo della biologia biomedica.
In parallelo, nuovi strumenti come l’ultracentrifuga, il microscopio elettronico e l’elettroforesi, permisero ai ricercatori di ideare dei protocolli metodologici adeguati allo studio delle macromolecole.
La nascita della genomica
Nel 1976, Walter Fiers stabilì per primo la sequenza nucleotidica completa di un genoma virale a RNA (batteriofago MS2) e nel 1977, Frederick Sanger completò il primo progetto di sequenziamento di un genoma a DNA, del fago ΦX174, costituito da sole 5386 paia di basi.
Grazie a queste scoperte, nei decenni successivi furono ideate altre tecniche di sequenziamento degli acidi nucleici, con l’espansione della genomica.
Farmaci biotecnologici e Progetto Genoma Umano
Nel 1982, un farmaco sintetizzato tramite tecniche di ingegneria genetica – l’insulina – fu rilasciato in commercio per la prima volta.
Nel 1993, Kary Mullis fu insignito del Premio Nobel per la Chimica insieme a Michael Smith per il suo lavoro sulla reazione a catena della polimerasi (Polymerase Chain Reaction – PCR), una tecnica essenziale utilizzata nella biologia biomedica.
Il Progetto Genoma Umano fu una delle più grandi imprese scientifiche della storia. Un gruppo internazionale di ricercatori si era posto l’obiettivo di studiare in modo esaustivo tutto il DNA (noto come genoma) di un gruppo selezionato di organismi. Avviato nell’ottobre del 1990 e completato nell’aprile del 2003, il Progetto Genoma Umano, con la generazione della prima sequenza del genoma umano, ha accelerato i progressi della biologia biomedica.
Attualmente, la biologia biomedica si occupa di capitalizzare le scoperte effettuate per offrire alla medicina degli inediti strumenti terapeutici.

Biologia biomedica e sviluppo di farmaci
La biologia biomedica ha promosso la scoperta di nuovi farmaci e di sistemi di somministrazione. In generale, un farmaco è una combinazione di uno o più principi attivi e di componenti non farmacologici chiamati eccipienti/additivi, che stabilizzano il principio attivo. L’obiettivo di qualsiasi sistema di somministrazione è indirizzare e confinare il farmaco nel tessuto malato.
Dopo l’assunzione di una singola dose di farmaco con formulazione convenzionale (compresse, capsule, sciroppi, etc.), il corpo umano metabolizza il farmaco rapidamente. Come risultato, la finestra temporale in cui il farmaco è presente nell’organismo nella dose efficace potrebbe non essere sufficiente a produrre l’effetto terapeutico desiderato.
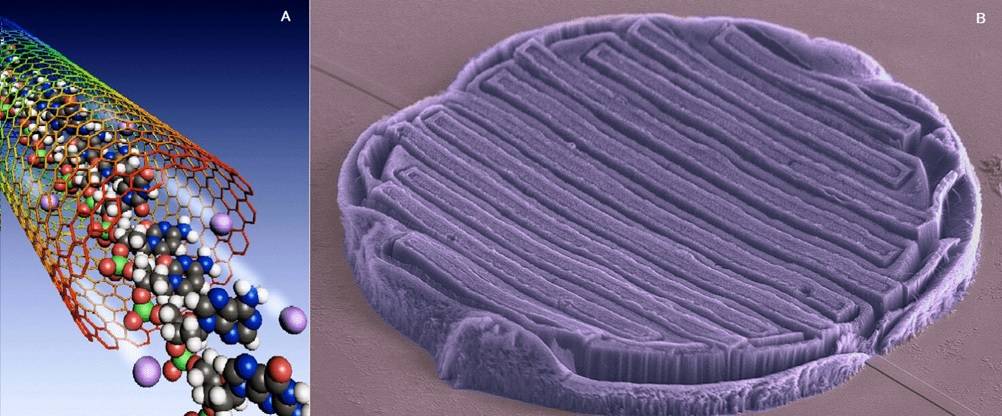
Allo scopo di migliorare l’azione dei principi attivi, la biologia biomedica, combinata con le nanotecnologie, ha ideato nuovi sistemi di somministrazione di farmaci.
Nanotecnologie
Le nanotecnologie prevedono l’impiego di sostanze su scala molto piccola. In generale, una sostanza chimica è considerata “nano” quando le sue dimensioni sono dell’ordine di 100 nm o inferiori.
Le nanosostanze offrono numerosi vantaggi rispetto ai farmaci tradizionali:
- aumentano la frazione di farmaco che raggiunge il circolo sanguigno, ovvero migliorano la biodisponibilità del farmaco;
- riducono gli effetti indesiderati dovuti al farmaco, perché la dose somministrata è inferiore;
- sono adeguati all’unione con molecole specifiche per il tessuto bersaglio, oppure possono racchiudere il principio attivo da rilasciare;
- sono differenziabili non solo per diversi tipi di cellule, ma anche per regioni specifiche di una cellula, ad esempio il nucleo.
Biologia biomedica e microbiologia
L’uso improprio o eccessivo di antibiotici ha condotto alla comparsa di batteri patogeni resistenti ai farmaci (antibiotico-resistenza). Senza antibiotici efficaci, il trattamento delle infezioni è quindi a rischio. Al fine di contrastare questo fenomeno, la biologia biomedica ha individuato delle nuove strategie.
Applicazioni biomediche dei peptidi antimicrobici
I peptidi antimicrobici sono una valida alternativa agli antibiotici tradizionali, perché agiscono contro batteri, funghi, lieviti e virus. I peptidi antimicrobici sono composti da 5-100 amminoacidi. Più di 2500 tipi di peptidi antimicrobici sono già presenti in natura in vertebrati, invertebrati e piante.
Fattori quali velocità di rilascio incontrollata, scarsa biocompatibilità, bassa solubilità, facilità di degradazione e tossicità sono limiti che la biologia biomedica sta cercando di superare, al fine di convertire i peptidi antimicrobici in farmaci.
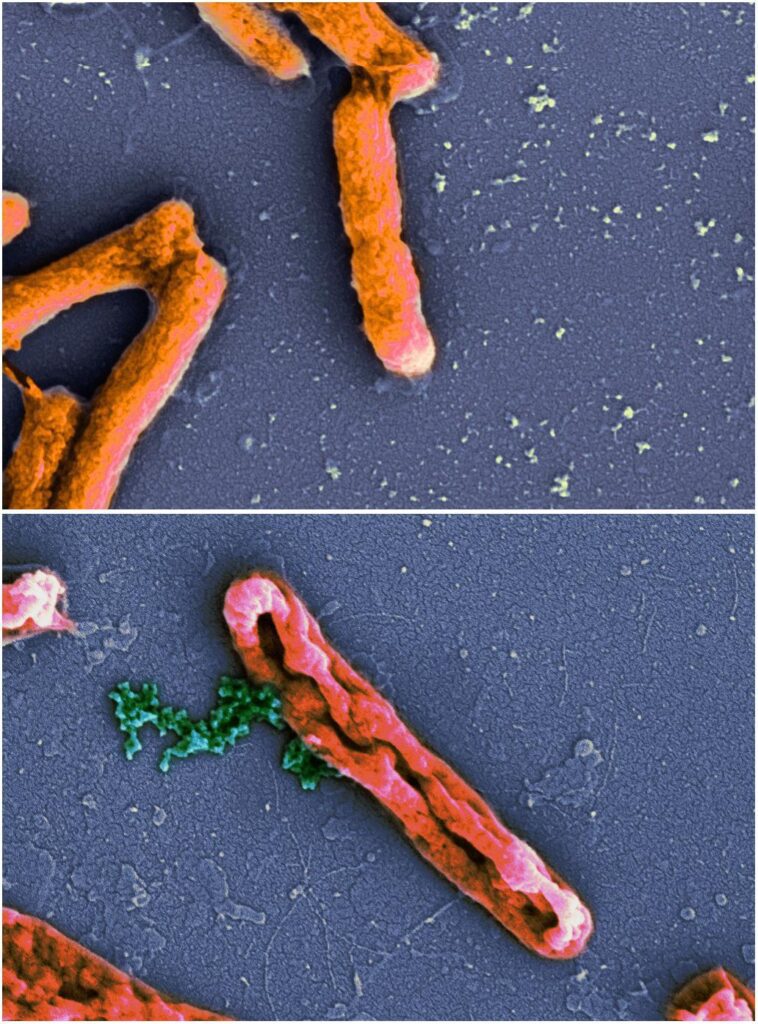
Peptidi antimicrobici e nanotecnologie
I patogeni ESKAPE sono responsabili della maggior parte delle infezioni ospedaliere potenzialmente letali. Oltre a questo, i patogeni “ESKAPE” sono resistenti ai farmaci; comprendono Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, incluse varie specie di Enterobacter.
Con l’obiettivo di individuare una soluzione all’antibiotico-resistenza, i ricercatori hanno così dimostrato che le nanoparticelle metalliche svolgono un’attività antibatterica contro i patogeni ESKAPE.
Le nanoparticelle di argento coniugate con peptidi antimicrobici rappresentano pertanto un campo di indagine promettente della biologia biomedica.
Biologia biomedica e oncologia
La biologia biomedica ha compreso i meccanismi della cancerogenesi e della metastasi.
Queste conoscenze sono state essenziali per progettare nuovi farmaci per bersagli molecolari tipici delle cellule tumorali, sviluppando strategie terapeutiche sempre più efficaci.
Nuove terapie contro il cancro
La chemioterapia “tradizionale” agisce in modo aspecifico sia sulle cellule tumorali che su quelle sane.
La terapia a bersaglio molecolare invece ha l’obiettivo di interferire solo con i processi cellulari delle cellule neoplastiche, utilizzando due tipi principali di farmaci: piccole molecole e anticorpi monoclonali.
Piccole molecole
Le “piccole molecole” sono composti chimici a basso peso molecolare (minore di 900 Dalton). Questi composti si legano a proteine che regolano il ciclo cellulare, l’apoptosi e la riparazione del DNA. Le piccole molecole sono di conseguenza capaci di bloccare la proliferazione delle cellule tumorali.
Anticorpi monoclonali
Gli anticorpi monoclonali sono proteine prodotte in laboratorio, in modo tale da riconoscere un solo antigene; agiscono su recettori di membrana o proteine extracellulari per bloccare la proliferazione delle cellule tumorali.
Ad esempio, trastuzumab è un anticorpo monoclonale diretto contro il recettore per il fattore di crescita epidermico umano-2 (HER2), che è sovraespresso in un sottogruppo di pazienti con cancro al seno e gastrico.

Biologia biomedica e immunologia
La biologia biomedica analizza la risposta immunitaria su più livelli. Come metodologia impiegata, la biologia biomedica si avvale delle tecnologie di sequenziamento degli acidi nucleici e della bioinformatica.
Indagare la risposta immunitaria con il sequenziamento dell’RNA
Gli studi sulle cellule singole hanno messo in luce sia la diversità delle sottopopolazioni cellulari, sia l’eterogeneità delle singole cellule appartenenti ad uno stesso tessuto. Al fine di raggiungere questi risultati, gli studi sulle cellule singole si sono basati, fra i vari metodi, sul sequenziamento del trascrittoma (o dell’RNA) delle singole cellule.
Impiegando soprattutto il sequenziamento del trascrittoma, i ricercatori hanno scoperto che nei tessuti vi sono diversi sottotipi di macrofagi. Analizzare i sottogruppi di macrofagi faciliterà in futuro la raccolta di nuove informazioni sulla risposta immunitaria e la progettazione di strategie terapeutiche sempre più efficaci.
Il sequenziamento dell’RNA ha dimostrato inoltre che l’enzima di conversione dell’angiotensina 2 (ACE2) è il recettore cruciale per il SARS-CoV-2. Infatti, le cellule che esprimono alti livelli di ACE2 sono più suscettibili all’infezione da SARS-CoV-2.

Conclusioni
La biologia biomedica ha condizionato profondamente la medicina. E’ probabile che i futuri medici avranno sempre più bisogno di conoscenze di biologia cellulare e molecolare, genomica ed immunologia per applicare i principi della medicina personalizzata nella pratica clinica.
L’aspettativa per il futuro è che la biologia biomedica possa convertire i risultati sperimentali raggiunti in trattamenti terapeutici accessibili alla popolazione mondiale.
Il costo dei nuovi farmaci biologici potrebbe infatti impedire a molti pazienti di ricevere delle cure essenziali. Lo sviluppo di farmaci rimane un’impresa costosa, nonostante gli sforzi in corso da parte di tutte le aziende farmaceutiche e biotecnologiche per contenere i crescenti costi. Poiché il processo di ricerca e sviluppo è caratterizzato da notevoli imprevisti tecnici, solo una parte degli investimenti sostenuti si traduce nell’approvazione all’autorizzazione in commercio dei farmaci.
Saranno quindi indispensabili degli interventi da parte delle organizzazioni che regolano la spesa farmaceutica, per sostenere gli sviluppi futuri della biologia biomedica.
Fonti
- Quirke V, et al., The era of biomedicine: science, medicine, and public health in Britain and France after the Second World War. Med Hist. 2008 Oct;52(4):441-52
- https://www.genome.gov/human-genome-project#:~:text=The%20Human%20Genome%20Project%20is,a%20select%20set%20of%20organisms.
- https://www.synthego.com/learn/genome-engineering-history
- https://www.unomaha.edu/college-of-arts-and-sciences/biology/academics/molecular-biomedical-biology.php#a
- Adepu, S. et al.; Controlled Drug Delivery Systems: Current Status and Future Directions. Molecules 2021, 26, 5905.
- https://www.efsa.europa.eu/it/topics/topic/nanotechnology#:~:text=Le%20nanotecnologie%20prevedono%20l’impiego,di%20100%20nm%20o%20inferiori.
- https://www.who.int/news-room/fact-sheets/detail/antimicrobial-resistance#:~:text=What%20is%20antimicrobial%20resistance%3F,spread%2C%20severe%20illness%20and%20death.
- Sultana, A. et al.; Antimicrobial Peptides and Their Applications in Biomedical Sector. Antibiotics 2021, 10,1094
- Makowski, M. et al.; Advances in Lipid and Metal Nanoparticles for Antimicrobial Peptide Delivery. Pharmaceutics 2019, 11, 588
- Mulani MS et al.; Emerging Strategies to Combat ESKAPE Pathogens in the Era of Antimicrobial Resistance: A Review, Front. Microbiol. 2019, 10:539
- Piña-Sánchez P et al.; Cancer Biology, Epidemiology, and Treatment in the 21st Century: Current Status and Future Challenges From a Biomedical Perspective. Cancer Control. January 2021
- Kaufmann SHE; Immunology’s Coming of Age. Front Immunol. 2019 Apr 3;10:684
- https://www.cancer.gov/publications/dictionaries/cancer-terms/def/monoclonal-antibody
- Luo G, et al; Probing infectious disease by single-cell RNA sequencing: Progresses and perspectives. Comput Struct Biotechnol J. 2020;18:2962-2971
Crediti immagini
- Immagine in evidenza: https://www.flickr.com/photos/nasamarshall/33350284091
- Figura 1: https://www.flickr.com/photos/rosenfeldmedia/49781638126/in/photostream/
- Figura 2A: https://www.flickr.com/photos/oakridgelab/4386875333
- Figura 2B: https://www.flickr.com/photos/zeissmicro/23007950410
- Figura 3: https://upload.wikimedia.org/wikipedia/commons/e/e7/AMP_action_Ecoli.jpg
- Figura 4: https://www.flickr.com/photos/nihgov/24190675263
- Figura 5: https://www.flickr.com/photos/niaid/33031032718